Six-minute walk test in patients hospitalized for heart failure with reduced ejection fraction.
Test de marche de six minutes chez les patients hospitalisés pour insuffisance cardiaque à fraction d'éjection du ventricule gauche réduit.
Sm LIMAME 1, MI ELKHARCHY 1, L BABA TALL 1, Sm ETHMAN 1, S CAMARA 1,
K BOYE 1, 2, A EBA ELWELATY 1, 3, H ZEIN 1,3.
RESUME
Introduction : Le pronostic de l'insuffisance cardiaque est lié à la capacité fonctionnelle pouvant être évaluée par des tests d'effort.
Objectif : L'objectif de notre travail est d'évaluer la valeur pronostique du test de marche de 6 minutes (TDM6) en termes de mortalité toutes causes confondues et de réhospitalisation pour insuffisance cardiaque chez les patients hospitalisés pour insuffisance cardiaque à fraction d'éjection du ventricule gauche (FEVG) réduite. Méthode : Il s'agit d'une étude observationnelle prospective et monocentrique avec une durée de suivi de 12 mois. Nous avons inclus tous les patients adultes hospitalisés au Centre National de Cardiologie pour IC à FEVG réduite pouvant bénéficier d'un TDM6. Résultats : Trente-huit patients hospitalisés pour insuffisance cardiaque à FEVG réduite étaient étudiés. L'âge moyen de nos patients était de 58,89 ± 16 ans. Les hommes représentaient 81,6%. Tous les patients étaient à un stade IIIb de la NYHA. La FEVG moyenne était de 27%. Le rythme cardiaque était sinusal chez 76,3% des patients. Le DFG moyen était de 65,53 ± 20 ml/min/1,73 m² et la BNP moyenne était de 6047 ± 9400 pg/ml. À la sortie de l'hôpital, 97,4% des patients étaient sous un inhibiteur de l'enzyme de conversion, 84,2% un bétabloquant, 89,5% un anti-aldostérone et 84,20 % avaient un inhibiteur du cotransporteur sodium glucose de type 2. La distance moyenne parcourue au cours du TDM6 était de 269 ± 102 m. La mortalité et la réhospitalisations pour IC à 1 an étaient respectivement de 23,68% et 36,8%. Une faible distance parcourue au cours du TDM6 à la sortie de l'hôpital avait prédit significativement le risque de décès (p= 0.019) et le risque de réhospitalisation pour IC (p= 0.011) à 12 mois. Le seuil optimal déterminé par la courbe ROC pour prédire ces évènements était une distance TDM6 égal à 250 m (Area under the curve (AUC) = 0.75; 95% CI = 0.55 – 0.95; p= 0,028 ; sensibilité de 0.72 et spécificité de 0.78). Pour les patients qui avaient marché une distance au cours du TDM6 ≤ 250 m, la mortalité était de 46,7% contre 8,7% chez les patients qui avaient marché une distance du TDM6 ˃250m (p=0,016). Pour les patients qui avaient marché une distance au cours du TDM6 ≤ 250 m, la réhospitalisation pour IC était de 64,3% contre 35,7% chez les patients qui avaient marché une distance du TDM6 ˃250m (p=0,037).
Conclusion : Le TDM6 est un marqueur pronostic simple, peu couteux et sûr qui peut prédire à court terme la mortalité toutes causes et la réhospitalisation pour IC chez les patients hospitalisés pour IC à FEVG réduite.
MOTS CLES
Insuffisance cardiaque, pronostic, exercice, test de marche.
SUMMARY
Introduction: The prognosis of heart failure is linked to functional capacity which can be assessed by exercise tests.
Purpose: The objective of our work is to evaluate the prognostic value of the 6-minute walk test in terms of all-cause mortality and rehospitalization for heart failure in patients hospitalized for heart failure with reduced ejection fraction (HFrEF).
Methods: This is was prospective, monocentric, and observational study with a follow-up duration of 12 months. We included all patients hospitalized at the National Cardiology Center for heart failure (HF) with reduced ejection fraction who could benefit from the 6-minute walk test.
Results: Thirty-eight patients hospitalized for heart failure with reduced ejection fraction were studied. The average age of our patients was 58.89 ± 16 years. Men represented 81.6%. All patients were at New York Heart Association stage IIIb. The mean left ventricular ejection fraction was 27%. Patients had sinus rhythm in 76.3%. The mean glomerular filtration rate was 65.53 ± 20 ml/min/1.73 m² and the mean brain natriuretic peptide was 6047 ± 9400 pg/ml. At hospital discharge, 97.4% of patients were on an angiotensin-converting enzyme inhibitor, 84.2% on a beta blocker, 89.5% on an anti-aldosterone inhibitor and 84.20% on a sodium glucose co-transporter 2 inhibitors. The average distance traveled during the 6-minute walk test was 269 ± 102 m. Mortality at 1 year was 23.68% and rehospitalization for HF at 1 year was 36.8%. A low distance traveled during the 6-minute walk test at hospital discharge significantly predicted the risk of death (p=0.019) and the risk of rehospitalization for HF (p=0.011). The optimal threshold determined by the Receiver Operating Characteristic (ROC) curve to predict these events was a 6-minute walk test distance equal to 250 m (Area under the curve (AUC) = 0.75; 95% CI = 0.55 – 0.95; p= 0,028 ; sensitivity of 0.72 and specificity of 0.78). For patients who had walked a distance during the 6-minute walk test ≤250 m, mortality was 46.7% compared to 8.7% in patients who had walked a distance during the 6- minute walk test ˃250m (p=0.016). For patients who had walked a distance during the 6-minute walk test ≤250 m, rehospitalization for HF was 64.3% compared to 35.7% in patients who had walked a distance during the 6-minute walk test ˃250m (p=0.037).
Conclusion: We conclude that 6-minute walk test is a simple, inexpensive, and safe prognostic marker that can predict short- term all-cause mortality and rehospitalization for HF in patients hospitalized for HFrEF.
KEY WORDS
Heart failure, prognosis, exercise, walk test.
1 Centre National de Cardiologie, Nouakchott, Mauritanie
2 Professeur en chirurgie cardiovasculaire, Faculté de médecine de Nouakchott-Mauritanie
3 Professeur en cardiologie, Faculté de médecine de Nouakchott-Mauritanie
Adresse pour correspondance
يد س محمد يخ ش ال اإلمام < This email address is being protected from spambots. You need JavaScript enabled to view it. >
mohamed issa kharchi < This email address is being protected from spambots. You need JavaScript enabled to view it. >
INTRODUCTION
L’insuffisance cardiaque (IC) est un problème de la santé publique mondiale (1). Elle se définit comme un syndrome clinique avec des symptômes et des signes causés par une anomalie cardiaque structurelle ou fonctionnelle corroborée par une élévation des taux de peptides natriurétiques et/ou des signes de congestion pulmonaire ou systémiques objectifs (2). Pour décrire l’IC, il est classique d’utiliser la fraction d’éjection du ventricule gauche (FEVG). L'American College of Cardiology (ACC) définit quatre catégories de l’IC selon la FEVG : IC à FEVG réduite, IC à FEVG moyennement altérée, IC à FEVG préservée et IC à FEVG améliorée. Les mêmes auteurs de ces recommandations répartissent l’IC selon l’évolution en quatre stades : stade A inclus les patients qui ont les facteurs de risque de l’IC, stade B pré-insuffisance cardiaque, stade C insuffisance cardiaque symptomatique et stade D insuffisance cardiaque avancée (3). Le pronostic de l’IC est sombre et certains auteurs comme Stewart (4) et Mamas (5) ont montré que le pronostic de l’IC est plus péjoratif que la majorité des cancers. Ce pronostic est strictement lié à la capacité fonctionnelle (6,7). L’estimation de ce pronostic par la morbidité et la mortalité aide les patients, les familles et les médecins à décider du type de thérapeutique et de son timing.
Les marqueurs pronostiques sont nombreux mais leur application clinique est limitée et la stratification du risque reste un défi.
L’épreuve d’effort cardiopulmonaire est un moyen précis pour le diagnostic et l’évaluation de l’IC car les symptômes de l’IC ont tendance à se manifester à l’effort et la consommation maximale d’oxygène (VO2) en particulier représente une mesure objective de la gravité de l’insuffisance cardiaque qui est reproductible et prédit de manière fiable le pronostic de l’IC (8). Mais l’utilisation de l’épreuve d’effort cardiopulmonaire dans la pratique courante est limitée par la non- disponibilité et son coût élevé. C'est ainsi que le test de marche de six minutes (TDM6) a été proposé pour l’évaluation indirect de la capacité fonctionnelle comme alternative à l’épreuve d’effort cardiopulmonaire car il est simple, sûr et peu couteux. L’utilité du TDM6 pour stratifier le pronostic de l’IC a été rapporté pour la premiere fois par Bittner chez les patients de l’étude SOLVD (9).
Cependant la valeur pronostique du TDM6 chez les patients en IC reste controversée (10,11).
L’objectif de notre étude était d’évaluer la valeur pronostique du TDM6 en termes de mortalité toutes causes et de réhospitalisation pour insuffisance cardiaque chez les patients hospitalisés dans notre service pour IC à FEVG réduite.
PATIENTS ET METHODES
Cadre d’étude
L’étude est déroulée au service d’hospitalisation adulte du Centre National de Cardiologie (CNC).
Le CNC est créé par le décret numéro 2009-044 du 28 janvier 2009, c’est un établissement public à caractère administratif, doté de la personnalité juridique et de l’autonomie financière.
Le service d’hospitalisation adulte est situé au deuxième étage du CNC. Il prend en charge les patients adultes nécessitant une hospitalisation pour des causes cardiovasculaires et il est répartie en secteur homme de 30 lits, un secteur femme de 21 lits, dix bureaux, deux salles de gardes, deux salles d’échographie et deux salles d’archive.
Le cadre personnel du service de l’hospitalisation adulte comprend dix cardiologues, des cadres paramédicaux et cadres administratifs.
Population étudiée
L’étude réalisée est une étude observationnelle descriptive et analytique de manière prospective et monocentrique (Centre National de Cardiologie). Les patients ont été inclus sur une période de trois mois à partir du 1er août jusqu’au 31 octobre 2022 avec un suivi de 12 mois ; ont été inclus les patients adultes hospitalisé dans le service d’hospitalisation adulte durant cette période pour insuffisance cardiaque à FEVG réduite capable de bénéficier d’un TDM6.
Les critères d'exclusion étaient l’infarctus du myocarde récent, l’angor instable, la maladie aortique sévère symptomatique, l'hypertension artérielle (HTA) non contrôlée, la thrombose veineuse profonde récente, l'embolie pulmonaire récente, l'instabilité hémodynamique, les troubles du rythme et de conduction graves, l'infection grave, l'anémie (HB≤12g/dl) et l'incapacité de réaliser un exercice physique.
Tous ces critères étaient retranscrits sur une feuille de recueil accompagnant chaque dossier de patient afin de s’assurer de l’absence de critère de non-inclusion.
Le recueil des données
Lors de l’hospitalisation dans le service de cardiologie adulte, on a recueilli pour chaque patient des données cliniques et paracliniques par les médecins du service et il a été proposé aux patients éligibles à notre étude de réaliser le TDM6 avant la sortie de l’hôpital.
Les données cliniques recueillies étaient l'âge, le sexe, les antécédents d’IC et de fibrillation auriculaire, les facteurs de risque cardiovasculaires modifiables (Tabac, diabète, HTA), le stade de la dyspnée selon la NYHA et les paramètres hémodynamiques (conscience, tension artérielle, fréquence cardiaque, saturation, diurèse). Les données électriques recueillies étaient le rythme cardiaque et les troubles du rythme et de conduction. Les paramètres de l’échocardiographie transthoracique (ETT) recueillies étaient la FEVG qui était calculée par la méthode de Simpson biplan, le diamètre télésystolique du ventricule gauche (DTSVG), le diamètre télédiastolique du ventricule gauche (DTDVG), le diamètre télédiastolique du ventricule droit, la fonction systolique du ventricule droit (FSVD) qui était estimée par une approche multiparamétrique par le calcul de la fraction de raccourcissement du ventricule droit, du TAPSE et l’onde S’t. Nous avions également mesuré les volumes des oreillettes, la pression artérielle pulmonaire systolique (PAPS) et les paramètres d’estimation des pressions de remplissage du ventricule gauche en doppler pulsé mitral (onde protodiastolique E et onde télédiastolique A) et en doppler tissulaire de l’anneau mitrale (onde Em la première onde diastolique). L’ETT nous a également renseigné sur l’étiologie de l’IC. Nous avons aussi relevé les données biologiques suivantes : urée, créatinémie, le débit de filtration glomérulaire à partir de l’équation MDRD, BNP, natrémie, CRP et Hb. La coronarographie était réalisée chez tous les patients de notre étude à la recherche de coronaropathie.
Nous avons ainsi recueilli le traitement de sortie de tous les patients de l’étude.
Le TDM6 était réalisé dans un couloir sur une distance de 30 m, chaque participant était invité à marcher (et non à courir) le long du couloir aussi rapidement que possible, de sorte que la plus longue distance possible soit parcourue en six minutes.
Le patient était autorisé à s’arrêter et se reposer si nécessaire, en particulier en cas de symptômes. Ainsi que toutes les deux minutes l’investigateur informe le patient du temps restant et l'encourage pour poursuivre le TDM6. Au bout de six minutes on conseillait au patient de s’arrêter et de s’assoir. L’investigateur mesurait immédiatement la pression artérielle, la fréquence cardiaque et la saturation artérielle après le TDM6.
Le médecin calculait ensuite la distance parcourue par le patient lors du TDM6.
On avait suivi les patients après le TDM6 pendant cinq heures dans une salle de surveillance équipée par un scope et un défibrillateur.
Suivi des patients
La durée de suivi été de 12 mois avec une évaluation réalisée par l’investigateur chaque 3 mois afin de rechercher la survenue d'un évènement cardiovasculaire majeur.
Critères d’évaluation
Les critères de jugement principal étaient :
- Mortalité toutes causes confondues ;
- La réhospitalisation pour IC.
Analyse statistique
Les données ont été saisies sur le logiciel IBM SPSS Statistics 23. Les variables quantitatives étaient rapportées sous formes de moyenne ± écart-type et les variables qualitatives ont été rapportées sous forme de pourcentage. La différence entre les variables était déterminée par les tests de Fisher et le test de khi deux. La méthode de Kaplan Meier était utilisée pour construire les courbes. Le modèle de Cox était utilisé pour estimer le risque relatif de décès toutes causes confondues et de réhospitalisation pour insuffisance cardiaque. La courbe ROC (Receiver Operating Characteristic) était utilisé pour évaluer la performance du TDM6. Une valeur de P<0,05 était considérée comme statistiquement significative.
Consentement
Chaque patient avait émis son consentement écrit autorisant l’investigateur à utiliser ses données en assurant qu’elles resteront anonymes.
RESULTATS
Population de l'étude
Nous avons colligé 38 patients avec une durée de suivi moyenne de 12 mois dont les caractéristiques étaient les suivantes :
Données épidémiologiques
L'âge moyen des patients était de 58,89 ± 16 ans, avec des extrêmes de 20 et 91 ans. Le genre masculin représentait 81,60% contre 18,40% des femmes soit un ratio de 4,43. Le tabagisme actif était retrouvé chez 26 patients soit 68,40%. L’HTA était retrouvée chez 17 patients soit 44,70% des patients. Le diabète était retrouvé chez 7 patients soit 18,40%. Douze patients soit 31,60% étaient suivis pour IC. Quatre patients soit 10,50% étaient en fibrillation auriculaire (FA). Seize patients soit 42,10% avaient une cardiopathie ischémique. Les autres patients avaient une cardiopathie dilatée.
Données cliniques
Tous les patients avaient une dyspnée stade IIIb de la NYHA. La pression artérielle systolique (PAS) moyenne était de 116,34 ± 20 mmHg avec des extrêmes de 90 et 170 mmHg. La pression artérielle diastolique (PAD) moyenne était de 72 ± 20 mmHg avec des extrêmes de 50 et 100 mmHg.
La fréquence cardiaque (Fc) moyenne était de 88 ± 14 bpm avec des extrêmes de 50 et 120. La saturation artérielle en oxygène (SaO2) en moyenne était de 97% avec des extrêmes de 92 et 100%. Tous les patients étaient sous les diurétiques de l’anse. Trente-sept patients soit 97,40% avaient un inhibiteur de l’enzyme de conversion. Trente-deux patients soit 84,20% avaient un bétabloquant validé dans le traitement de l’insuffisance cardiaque. Trente- quatre patients soit 89,50% avaient un inhibiteur de l’aldostérone. Trente-deux patients soit 84,20 avaient un inhibiteur du cotransporteur sodium-glucose de type 2.
Electrocardiogramme (ECG)
Le rythme cardiaque était sinusal chez vingt- neuf patients soit 76,30% contre neuf patients soit 23,70% qui avaient une fibrillation atriale. Dix patients soit 26,30% avaient un bloc de brache gauche (BBG), deux patients soit 5,30% avaient un bloc de brache droit (BBD) et un patient avait un bloc auriculoventriculaire de premier degré (BAV I). Huit patients soit 21,10% avaient des extrasystoles ventriculaires (ESV) polymorphes.
Biologie
Tous les patients avaient un taux d'HB supérieur à 12 g/dl. La créatininémie moyenne était de 14,26 ± 4 mg/l avec des extrêmes entre 7,89 et 27,40 mg/l. Le taux d'urée dans le sang moyenne était de 0,55 ± 0,39 g/l avec des extrêmes entre 0,17 et 2,30 g/l. Le débit de filtration glomérulaire (DFG) moyenne était de 65,53 ± 20 ml/min/1,73 m² avec des extrêmes entre 29 et 105 ml/min/1,73 m². La natrémie moyenne était de 136 ± 5 meq/l avec des extrêmes entre 118 et 142 meq/l. La BNP moyenne était de 6047 ± 9400 pg/ml avec des extrêmes entre 50 et 25000 pg/ml. La CRP moyenne était de 54 ± 41 mg/l avec des extrêmes entre 6 et 140 mg/l.
Echocardiographie transthoracique
La fraction d’éjection ventriculaire gauche moyenne était de 27% +/- ET avec des extrêmes de 15 et 38%. Le diamètre télédiastolique du ventricule gauche (DTDVG) moyen était de 68 ± 8 mm avec des extrêmes entre 43 et 79 mm. Le diamètre télésystolique du ventricule gauche (DSDVG) moyen était de 51 ± 8 mm avec des extrêmes entre 35 et 73 mm. Chez les patients en rythme sinusal, le rapport E/A moyen était de 2,14 ± 1,12. Le rapport E/Em moyen était de 18,02 ± 12,33. Tous les patients avaient une oreillette gauche dilatée. Vingt-et-un patients soit 55,30% avaient une oreillette droite dilatée. Le ventricule droit était dilaté chez dix-sept patients soit 44,70%. La fonction du ventricule droit était altérée chez treize patients soit 34,20%. La pression artérielle pulmonaire systolique (PAPS) moyenne était de 50 ± 19 mmHg ( Tableau 1).
Test de marche de six minutes
La distance parcourue au cours du TDM6 moyenne était de 269 ± 102 m avec des extrêmes entre 72 et 480m. La pression artérielle systolique moyenne était de 122 ± 19 mmHg avec des extrêmes entre 90 et 182 mmHg. La pression artérielle diastolique moyenne était de 76 ± 15 mmHg avec des extrêmes entre 50 et 130 mmHg. La fréquence cardiaque moyenne était de 100 ± 18 bpm avec des extrêmes entre 60 et 157 bpm. La saturation artérielle d’oxygène moyenne était de 95 ± 6% avec des extrêmes entre 70 et 100%. Le pourcentage des patients sous bétabloquants chez les patients qui avaient marché une distance au cours du TDM6 ≤250 m était 31,3% contre 68,7% chez les patients qui avaient marché une distance au cours du TDM6 ˃250m avec une différence significative p=0,027. La valeur du BNP moyenne chez les patients qui avaient marché une distance au cours du TDM6 ≤250 m était de 12553±17602 pg/ml contre 4104±7544 pg/ml chez les patients qui avaient marchés une distance au cours du TDM6 ˃250m avec une différence significative p=0,047. La fréquence cardiaque moyenne après le TDM6 chez les patients qui ont marché une distance au cours du TDM6 ≤250 m était de 65 ± 7 bpm contre 106 ±14 bpm chez les patients qui avaient marché une distance au cours du TDM6 ˃250m avec une différence significative p=0,04. Les autres paramètres sont représentés dans le tableau 2.
Evènements cliniques majeurs après le test de marche de six minutes
Au cours de la surveillance hospitalière après le TDM6, un seul patient soit 2,63% des cas avait une tachycardie ventriculaire avec instabilité hémodynamique.
Suivi
Décès
La mortalité à 12 mois était de 23,68% (9 patients). L'âge moyen des décès était de 67±7 ans contre 56 ±18 ans chez les vivants avec une différence significative p=0,049. Les valeurs moyennes de l'urémie et de la créatininémie chez les décès étaient respectivement 0,86±0,6 g/l et 17,34±4 mg/l contre 0,45±0,2 g/l et 13,31±4 mg/l chez les vivants avec des différences significatives respectivement p=0,013 et p=0,006. La DFG moyenne chez les décès était de 51,44±12 ml/min/1,73 m² contre 69,9±20 ml/min/1,73 m² chez les vivants avec une différence significative p=0,016. La distance moyenne du TDM6 chez les patients décédés était de 200±96 m contre 290 ± 96 m chez les vivants avec une différence significative p=0,025. La courbe d'analyse ROC (receiver operating characteristic) qui indique la valeur de la distance du TDM6 pour prédire la mortalité à 1 an est representé dans la figure 1. Pour la distance de TDM6 [Area under the curve (AUC) = 0.75; 95% CI = 0.55 – 0.95; p=0,028], le cut-point optimal pour prédire la mortalité était 250 m avec une sensibilité de 0.86 et une spécificité de 0.81. L'analyse de survie par la courbe de Kaplan-Meier pour prédire la probabilité du décès en fonction de la distance du TDM6 ≤ 250 m et ≥ 250m est représenté dans la figure 2. Chez les patients qui ont marchés une distance du TDM6 ≤ 250m, le pourcentage du décès était 46,7% contre 8,7% chez patients qui ont marché une distance ˃ 250 m avec une différence significative p=0,016 Les autres caractéristiques sont représentées dans le tableau 3.
Réhospitalisation pour insuffisance cardiaque
A 12 mois, quatorze patients soit 36,80% étaient réhospitalisés pour IC L'âge moyen des patients réhospitalisés pour IC était de 65±12 ans contre 55±18 ans chez les non réhospitalisés pour IC avec une différence significative p=0,041. La distance moyenne du TDM6 chez les patients réhospitalisés pour IC était de 235±108 m contre 335±75 m chez les patients non réhospitalisés pour IC avec une différence significative p=0,047.
La courbe d'analyse ROC (receiver operating characteristic) représenté dans la figure 3. Pour la distance de TDM6 [Area under the curve (AUC) = 0.7; 95% CI = 0.51 – 0.87; p 0,049], le cut-point optimal pour prédire la rehospitalistion pour IC était 250 m avec une sensibilité de 0.75 et une spécificité de 0.64. L'analyse de survie par la courbe de Kaplan- Meier pour prédire la probabilité de rehospitalisation en fonction de la distance du TDM6 ≤ 250 m et ≥ 250m est représenté dans la figure 4. Chez les patients qui avaient marché une distance du TDM6 ≤ 250 m, la réhospitalisation était de 64,3% contre 35,7% chez les patients qui avaient marché une distance du TDM6 ˃ 250 m avec une différence significative p=0,037. Les autres caractéristiques sont représentées dans le tableau 6. A l'analyse univarié par la régression COX, le risque de réhospitalisation pour IC était plus élevé chez les patients qui avaient une distance TDM6 ≤ 250 m comparablement avec ceux qui avaient une distance TDM6 supérieur à 250m avec une différence significative (HR= 6,321, p=0,012). Les autres paramètres sont représentés dans le tableau 7.
DISCUSSION
Notre étude décrit la valeur pronostique du TDM6 chez les patients hospitalisés pour insuffisance cardiaque à FEVG réduite. Le pronostic des patients en insuffisance cardiaque est modulé par des facteurs démographiques, fonctionnels, hémodynamiques et neurohormonales (12). Tous ces facteurs étaient pris en considération dans notre étude pour prédire la valeur pronostique chez les patients de notre série. La capacité fonctionnelle et la tolérance à l'effort sont des facteurs importants dans l'évaluation clinique chez les patients en IC. Le TDM6 est un test d'effort sous maximal qui identifie la limitation de la capacité fonctionnelle dans la vie quotidienne (13,14). Chez les patients en IC à un stade avancée le TDM6 peut être considérée comme un test d'effort maximal car leur activité quotidienne est proche à leur capacité d'effort maximale (15,16). L'âge moyen de notre étude (58,89 ans) était similaire à celui retrouvé par les études de alahdab MT (17), Rubim (18) et Gerald Roul (15) qui avaient des moyennes d'âge respectivement de 55 ans, 58 ans et 59 ans. Les femmes représentaient 18,4% des patients dans notre série. Dans les séries de Shah (19) et Alahdab MT (17) les femmes représentaient respectivement 20% et 36,9%. La cardiopathie ischémique représentait 42,1% dans notre série. Dans les séries de Naïbé Dangwé Temoua (20), Alahdab MT (17), et Shah (19) la cardiopathie ischémique représentaient respectivement 16,4%, 16,8%, et 67%. Cette différence n’était pas inétendue car des études antérieurs avaient montré que l’étiologie de l’insuffisance cardiaque chez les africains de race noire est le plus souvent l’hypertension artérielle. Tous les patients de notre série étaient en classe IIIb de la NYHA. Les auteurs Rubim (18), Naïbé Dangwé Temoua (20), Carlo Rostagno (10), Sakir Arslan (21), alahdab MT (17) et Shah (19) avaient des classes de NYHA III et IV respectivement de 3%, 24,6%, 32%, 39,5% 67% et 100%. La FEVG moyenne dans notre série était de 27,6%. Dans les séries de Opasich (22) et Curtis (11) la FEVG moyenne était respectivement de 26% et 34%. La mortalité toutes causes confondues dans notre étude (23,68%) était comparable à celle retrouvés par les études de Curtis JP (11) et alahdab MT (17) et Rostagno C (10) avec un pourcentage de décès respectivement de 26%, 29,8% et 34%. Nous avions observé qu'une distance parcourue au cours du TDM6 plus court à la sortie de l'hôpital après optimisation du traitement médical était significativement associé au décès toutes causes (p=0.019). La meilleure valeur seuil du TDM6 qui avait prédit la mortalité à 12 mois était de 250 m (p=0.028). La courbe ROC a déterminé la valeur seuil optimale pour les variables numériques sélectionnées par la méthode de régression logistique et il était clair que la distance parcourue au cours du TDM6 peut déterminer et participer avec d'autres paramètres à l'évaluation du pronostic des patients hospitalisés pour IC à FEVG réduite. Bien que la valeur pronostique du TDM6 observée était cohérente avec les résultats de nombreuses études (9,11,18,21). D'autres études n'ont trouvé aucune valeur pronostique du TDM6 (15,22,23). Les premières études réalisées pour évaluer la valeur pronostique du TDM6 chez les patients en IC avec des stades II et III de la NYHA ont montré que le TDM6 peut prédire significativement la mortalité dans les analyses univariées mais pas dans les analyses multivariées (15,22). Une troisième étude menée chez les patients en IC avancée a conclu que le TDM6 ne pouvait pas prédire de manière significative la survie chez ces patients (10). Le manque de signification pronostique du TDM6 dans ces études pourrait être lié à l'incorporation de VO2 max dans les analyses multivariées (17) et par le fait que la technique de remarques encourageantes n'étaient pas réalisés (18). L'encouragement des patients au cours du TDM6 améliorent la reproductibilité du TDM6 (24). Tous les patients de notre série avaient bénéficié de la technique d'encouragement au cours de la réalisation du TDM6. La distance parcourue au cours du TDM6 qui prédit la mortalité toute cause confondue par notre étude (250m) semble être inférieur à celle retrouvée par d'autres études dont la plupart ont trouvé un seuil de 300 m qui détermine de manière fiable les patients à haut risque d'évènement cardiovasculaire (9,10,12,15,20,21). Ce qui peut s'expliquer par le fait que nos patients étaient à un stade avancé de l'IC et avec des valeurs assez faibles de la FEVG. D'autres auteurs avaient trouvé un seuil optimal de 200 m pour identifier les patients à haut risque de décès (11,17,25). Certains auteurs ont montré que le TDM6 peut identifier les patients à risque de congestion clinique (26) en particulier chez les sujets âgés qui développent généralement des symptômes à une capacité inférieure à leur capacité d'exercice maximale (27). D'autres ont montré que le TDM6 reflète également de nombreux paramètres telle que le débit cardiaque, la force musculaire squelettique, les comorbidités et l'état mental qui jouent en rôle pour le lien entre une distance courte parcourue au cours du TDM6 et la mortalité (25,26,28). La réhospitalisation pour IC était importante dans la plupart des séries quel que soit leurs performances sur le TDM6. Dans les séries de McCabe (26) et Shah (19) le taux de rehospitalisation pour IC était respectivement de 19% et 59%. Dans notre série le taux de réhospitalisation pour IC était de 36,8%. Cependant le rôle du TDM6 dans la prédiction de la réhospitalisation pour IC entant qu'évènement indépendant n'a pas été clairement établi. Des rares études sur ce sujet ont été limités par des petits échantillons et des durées de suivi relativement courte (9,11,26). Cependant Matsumoto K (25) dans l'essai Warcef trial avait objectivé qu'une distance du TDM6 inférieure ou égale à 200 m prédit le risque d'hospitalisation pour IC chez les patients stable en IC à FEVG réduite. De même Fatima Arhlade et al.(29) Avaient objectivé que le TDM6 prédit significativement chez les IC en ambulatoire le risque d'hospitalisation pour une décompensation cardiaque. Shah (19) avait montré que le TDM6 prédit significativement le risque de réhospitalisation chez les patients en IC avancée.
Nos données avaient révélé qu'une faible distance parcourue au cours du TDM6 est corrélée au risque de réhospitalisation pour IC (p=0.011) et qu'une distance inférieure ou égale à 250 m peut prédire d'une façon significative le risque de réhospitalisation pour IC (p=0.049). Ces résultats suggèrent l'utilité du TDM6 pour stratifier le risque de rehospitalisation pour IC chez les patients hospitalisés pour IC à FEVG réduite.
Le TDM6 a été suggéré comme un test sur, simple et peu couteux pour évaluer la capacité fonctionnelle chez les insuffisances cardiaques (17,25). Dans notre série une seule arythmie grave a été enregistrée au cours de la surveillance dans les 5H suivant la réalisation du TDM6. Les arythmies peuvent compromettre la surveillance des patients au cours du TDM6 car le patient n'est pas sous surveillance électrique continue(18). Cependant lors de l'étude SOLVD aucune arythmie n'a été enregistrée (9).
Anderson et al (30) ont montré que le taux de mortalité chez les insuffisances cardiaques sur cardiopathies ischémiques a été plus élevé que le taux de mortalité dans les autres causes d'IC. Dans notre série le taux de mortalité chez les IC sur cardiopathie ischémique a été plus faible que le taux de mortalité dans les autres causes. Ce qui pourrait être expliqué par une meilleure prise en charge des maladies coronaires.
CONCLUSION
Le TDM6 est un marqueur pronostique simple, peu couteux et sûr qui peut prédire à court terme la mortalité toutes causes et la réhospitalisation pour IC chez les patients hospitalisés pour IC à FEVG réduite.
Limites de l'étude :
La présente étude comporte plusieurs limites. Parmi ces limites : La petite taille de l'échantillon, La courte durée de suivi, Étude monocentrique. Ce qui pourrait réduire la puissance statistique des résultats pronostiques.
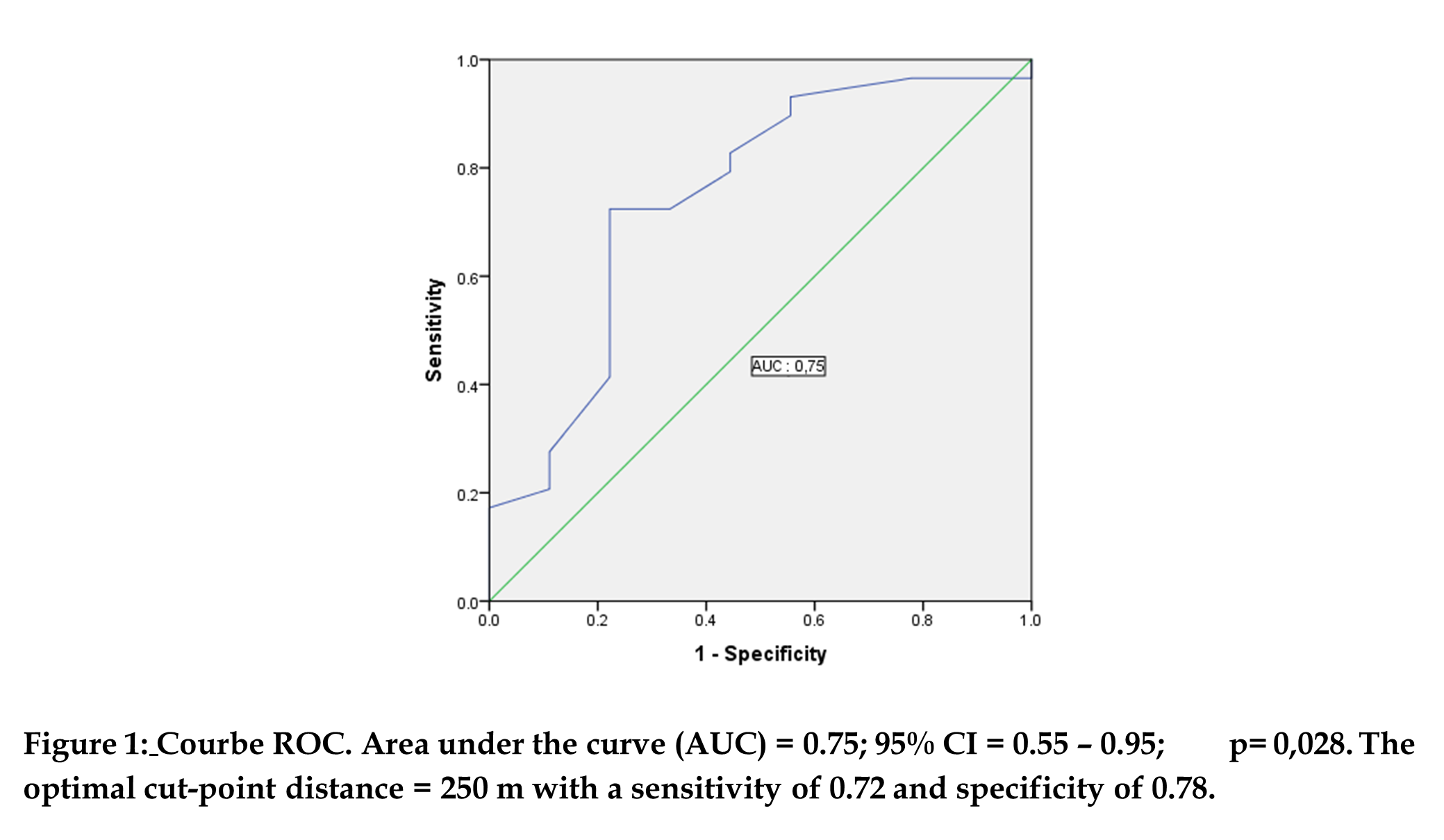
Tableau 1
Caractéristiques des patients
|
Caractéristiques des patients |
Nombre d'observation |
Moyenne et écart-type ou pourcentage |
|
Age (ans) |
38 |
58,89 ± 16 |
|
Les hommes (%) |
38 |
81,60 |
|
Couverture sanitaire (%) |
38 |
68,40 |
|
HTA (%) |
38 |
44,70 |
|
Tabac (%) |
38 |
68,40 |
|
Diabète (%) |
38 |
18,40 |
|
Antécédant IC (%) |
38 |
31,60 |
|
Antécédant FA (%) |
38 |
10,50 |
|
Etiologies IC Cardiopathie ischémique (%) |
38 |
42,10 |
|
NYHA IIIb (%) |
38 |
100 |
|
PAS (mmHg) |
38 |
116,34 ± 20 |
|
PAD (mmHg) |
38 |
72 ± 20 |
|
Fc (bpm) |
38 |
88 ± 14 |
|
BB (%) |
38 |
84,20 |
|
IEC (%) |
38 |
97,40 |
|
Aldactone (%) |
38 |
89,50 |
|
iSGLT2 (%) |
38 |
84,20 |
|
Rythme cardiaque Rythme sinusale (%) FA (%) |
38 |
76,30 23,70 |
|
BBG (%) |
38 |
26,30 |
|
BBD (%) |
38 |
5,30 |
|
ESV % |
38 |
21,10 |
|
Urée (g/l) |
38 |
0,55 ± 0,39 |
|
Créatininémie (mg/l) |
38 |
14,26 ± 4 |
|
DFG (ml/min/1,73 m²) |
38 |
65,53 ± 20 |
|
BNP (pg/ml) |
17 |
6047 ± 9400 |
|
Natrémie (meq/l) |
38 |
136 ± 5 |
|
CRP (mg/l) |
38 |
54 ± 41 |
|
FEVG (%) |
38 |
27 ± 6 |
|
DTSVG (mm) |
38 |
51 ± 8 |
|
DTDVG (mm) |
38 |
68 ± 8 |
|
FSVD Altérée (%) |
38 |
34,20 |
|
E/A |
38 |
2,14 ± 1,12 |
|
E/Em |
38 |
18,02 ± 12,33 |
|
PAPS (mmHg) |
38 |
50 ± 19 |
|
Distance parcourue (m) |
38 |
269 ± 102 |
|
PAS (mmHg) |
38 |
122 ± 19 |
|
PAD (mmHg) |
38 |
76 ± 15 |
|
Fc (bpm) |
38 |
100 ± 18 |
|
Evènements majeurs liés du TDM6 (%) |
38 |
2,63 |
BB : bétabloquant, BBG : bloc de branche gauchem ; BNP: B-type natriuretic peptide; CRP : protéine C-réactive; DFG : débit de filtration glomérulaire ; DTDVG : diamètre télédiastolique du ventricule gauche; DTSVG : diamètre télésystolique du ventricule gauche; ESV : extrasystole ventriculaire; FA : fibrillation auriculaire; Fc : fréquence cardiaque; FEVG : fraction éjection du ventricule gauche; FSVD : fonction systolique du ventricule droit; HTA : hypertension artérielle; IC : insuffisance cardiaque; IEC : inhibiteur de l'enzyme de conversion, ISGLT2: Sodium- glucose transport protein 2 inhibitors; NYHA: new york heart association; PAD : pression artérielle diastolique; PAPS: pression artérielle pulmonaire systolique, PAS : pression artérielle systolique; TDM6 : test de marche de six minutes
Tableau 2
Caractéristiques des patients hospitalisés pour insuffisance cardiaque à FEVG réduite accordés à la distance de TDM6
|
Caractéristiques des patients |
Distance TDM6≤250m |
Distance TDM6 ˃250m |
P-value |
|
Nombre des patients |
15 |
23 |
|
|
Age (ans) |
56±5 |
55±23 |
0,018 |
|
Les hommes (%) |
93,3 |
73,9 |
0,209 |
|
Antécédant IC (%) |
46,7 |
21,7 |
0,157 |
|
Etiologies IC Cardiopathie ischémique (%) |
46,7 |
39,1 |
0,743 |
|
PAS (mmHg) |
95±7 |
112±16 |
0,303 |
|
Fc (bpm) |
102±5 |
91±9 |
0,511 |
|
BB (%) |
66,7 |
95,7 |
0,027 |
|
IEC (%) |
93,3 |
100 |
0,395 |
|
Aldactone (%) |
86,7 |
91,3 |
1 |
|
iSGLT2 (%) |
80 |
87 |
0,663 |
|
FA (%) |
40 |
13 |
0,115 |
|
BBG (%) |
33,3 |
21,7 |
0,631 |
|
Urée (g/l) |
1,45±1 |
0,38±1 |
0,094 |
|
Créatininémie (mg/l) |
21,07±8 |
12,47±3 |
0,215 |
|
DFG (ml/min/1,73 m²) |
45±22 |
69,82±16 |
0,175 |
|
BNP (pg/ml) |
12553±17602 |
4104±7544 |
0,047 |
|
CRP (mg/l) |
61±39 |
59±50 |
0,495 |
|
FEVG (%) |
26,5±9 |
25,27±7 |
0,187 |
|
DTSVG (mm) |
55,5±4 |
52,27±9 |
0,16 |
|
DTDVG (mm) |
63,5±2 |
61,55±9 |
0,203 |
|
FSVD Altérée (%) |
53,3 |
21,7 |
0,079 |
|
E/A |
3,09±0,57 |
1,91±1,26 |
0,956 |
|
E/Em |
13,22±3 |
20±17 |
0,998 |
|
PAPS (mmHg) |
40±7 |
44±22 |
0,218 |
|
PAS après TDM6 (mmHg) |
98±11 |
120±11 |
0,138 |
|
PAD après TDM6 (mmHg) |
80±28 |
74±11 |
0,133 |
|
Fc après TDM6 (bpm) |
65±7 |
106±14 |
0,04 |
|
Mortalité à 1 an (%) |
46,7 |
8,7 |
0,016 |
|
Réhospitalisation pour IC à 1 an (%) |
60 |
21,7 |
0,037 |
BB : bétabloquant, BBG : bloc de branche gauchem ; BNP: B-type natriuretic peptide; CRP : protéine C-réactive; DFG : débit de filtration glomérulaire ; DTDVG : diamètre télédiastolique du ventricule gauche; DTSVG : diamètre télésystolique du ventricule gauche; ESV : extrasystole ventriculaire; FA : fibrillation auriculaire; Fc : fréquence cardiaque; FEVG : fraction éjection du ventricule gauche; FSVD : fonction systolique du ventricule droit; HTA : hypertension artérielle; IC : insuffisance cardiaque; IEC : inhibiteur de l'enzyme de conversion, ISGLT2: Sodium-glucose transport protein 2 inhibitors; NYHA: new york heart association; PAD : pression artérielle diastolique; PAPS: pression artérielle pulmonaire systolique, PAS : pression artérielle systolique; TDM6 : test de marche de six minutes
Tableau 3
Caractéristiques des patients hospitalisés pour IC à FEVG réduite accordés au décès
|
Caractéristiques des patients |
Les vivants |
Décès |
P-value |
|
Nombre des patients |
29 |
9 |
|
|
Age (ans) |
56 ±18 |
67±7 |
0,049 |
|
Les hommes (%) |
75,9 |
100 |
0,164 |
|
HTA (%) |
44,8 |
44,4 |
1 |
|
Tabac (%) |
65,5 |
77,8 |
0,689 |
|
Diabète (%) |
20,7 |
11,1 |
1,000 |
|
Antécédant IC (%) |
31,0 |
33,3 |
1,000 |
|
Etiologies IC Cardiopathie ischémique(%) |
41,4 |
44,4 |
1 |
|
PAS (mmHg) |
118±21 |
110±19 |
0,226 |
|
PAD (mmHg) |
73±12 |
67±12 |
0,196 |
|
Fc (bpm) |
87±13 |
92±16 |
0,208 |
|
BB (%) |
86,2 |
77,8 |
0,613 |
|
IEC (%) |
96,6 |
100,0 |
1 |
BB : bétabloquant, BBG : bloc de branche gauchem ; BNP: B-type natriuretic peptide; CRP : protéine C-réactive; DFG : débit de filtration glomérulaire ; DTDVG : diamètre télédiastolique du ventricule gauche; DTSVG : diamètre télésystolique du ventricule gauche; ESV : extrasystole ventriculaire; FA : fibrillation auriculaire; Fc : fréquence cardiaque; FEVG : fraction éjection du ventricule gauche; FSVD : fonction systolique du ventricule droit; HTA : hypertension artérielle; IC : insuffisance cardiaque; IEC : inhibiteur de l'enzyme de conversion, ISGLT2: Sodium-glucose transport protein 2 inhibitors; NYHA: new york heart association; PAD : pression artérielle diastolique; PAPS: pression artérielle pulmonaire systolique, PAS : pression artérielle systolique; TDM6 : test de marche de six minutes
Tableau 4
Analyse univariée COX qui prédit la mortalité chez les patients hospitalisés pour insuffisance cardiaque à FEVG réduite
|
Caractéristiques des patients |
Wald test |
HR |
95% IC |
P-value |
|
Age (ans) |
2,69 |
1,037 |
0,993-1,083 |
0,096 |
|
Les hommes |
0,91 |
28,881 |
0,28-29423 |
0,381 |
|
PAS |
0,78 |
0,982 |
0,944-1,022 |
0,378 |
|
PAD |
1,31 |
0 ,968 |
0,915-1,024 |
0,253 |
|
Fc |
0,802 |
1,026 |
0,970-1,085 |
0,37 |
|
FA (%) |
2,67 |
0,334 |
0,089-1,245 |
0,102 |
|
ESV % |
1,393 |
2,308 |
0,576-9,254 |
0,238 |
|
Urémie |
6,847 |
3,797 |
1,398-10,314 |
0,009 |
|
Créatininémie |
5,69 |
1,141 |
1,024-1,272 |
0 ,017 |
|
DFG |
5,637 |
0,951 |
0,912-0,991 |
0 ,018 |
|
BNP |
1,975 |
1 |
1-1 |
0,16 |
|
CRP |
1,759 |
1,010 |
0,995-1,025 |
0,185 |
|
FEVG (%) |
0,167 |
1,021 |
0,925-1,126 |
0,685 |
|
DTSVG |
0,298 |
1,021 |
0,948-1,098 |
0,585 |
|
DTDVG |
0,102 |
1,012 |
0,939-1,091 |
0,749 |
|
FSVD Altérée (%) |
2,355 |
0,357 |
0,096-1,331 |
0,125 |
|
E/A |
0,517 |
1,281 |
0,652-2,520 |
0,472 |
|
E/Em |
0,018 |
1,004 |
0,953-1,057 |
0,894 |
|
PAPS |
0,743 |
0,985 |
0,953-1,019 |
0,389 |
|
Distance parcourue |
5,493 |
0,992 |
0,985-0,999 |
0,019 |
|
Distance TDM6 ≤250 m |
5,816 |
6,940 |
1,437-33,505 |
0,016 |
|
PAS après TDM6 |
2,157 |
0,967 |
0,925-1,011 |
0,142 |
|
PAD après TDM6 |
0,938 |
0,974 |
0,922-1,028 |
0,333 |
|
Fc après TDM6 |
1,337 |
0,978 |
0,941-1,016 |
0,247 |
BB : bétabloquant, BBG : bloc de branche gauchem ; BNP: B-type natriuretic peptide; CRP : protéine C-réactive; DFG : débit de filtration glomérulaire ; DTDVG : diamètre télédiastolique du ventricule gauche; DTSVG : diamètre télésystolique du ventricule gauche; ESV : extrasystole ventriculaire; FA : fibrillation auriculaire; Fc : fréquence cardiaque; FEVG : fraction éjection du ventricule gauche; FSVD : fonction systolique du ventricule droit; HR: Hazard ration ; HTA : hypertension artérielle;; IC: intervalle de confiance; IEC : inhibiteur de l'enzyme de conversion, ISGLT2: Sodium-glucose transport protein 2 inhibitors; NYHA: new york heart association; PAD : pression artérielle diastolique; PAPS: pression artérielle pulmonaire systolique, PAS : pression artérielle systolique; TDM6 : test de marche de six minutes.
Tableau 5
Analyse multivariée COX régression des facteurs associées au décès
|
Caractéristiques des patients |
|
Décès |
|
|
|
HR |
95% IC |
P value |
|
Urémie |
1,410 |
0,210- 9,473 |
0,724 0,836 0,323 0,061 |
|
Créatininémie |
0,959 |
0,644- 1,427 |
|
|
DFG |
0,954 |
0,868- 1,048 |
|
|
Distance parcourue ≤ 250 m |
5,075 |
0,930- 27,697 |
DFG : débit de filtration glomérulaire ; HR: Hazard ration ; IC: intervalle de confiance.
Tableau 6
Caractéristiques des patients hospitalisés pour insuffisance cardiaque à FEVG réduite accordés à la réhospitalisation pour IC
|
Caractéristiques des patients |
Non réhospti |
rehospit |
P-value |
|
Nombre des patients |
24 |
14 |
|
|
Age (ans) |
55±18 |
65±12 |
0 ,041 |
|
Les hommes (%) |
70,8 |
100 |
0,033 |
|
HTA (%) |
45,8 |
42,9 |
1 |
|
Tabac (%) |
62,5 |
78,6 |
0,472 |
|
Diabète (%) |
20,8 |
14,3 |
1 |
|
Antécédant IC (%) |
25 |
42,9 |
0,296 |
|
Etiologies IC Cardiopathie ischémique (%) |
57,1 |
33,3 |
0,184 |
|
PAS (mmHg) |
118±21 |
112±18 |
0,413 |
|
PAD (mmHg) |
75±11 |
62±12 |
0,037 |
|
Fc (bpm) |
92±7 |
94±13 |
0,9 |
|
BB (%) |
88,3 |
85,7 |
1 |
|
IEC (%) |
95,8 |
100 |
1 |
|
Aldactone (%) |
87,5 |
92 ;9 |
1 |
|
iSGLT2 (%) |
83,3 |
85,7 |
1 |
|
FA (%) |
16,7 |
33,7 |
0,245 |
|
BBG (%) |
25 |
28,6 |
1 |
|
ESV % |
20,8 |
21,4 |
1 |
|
Urémie (g/l) |
0,38±0,14 |
0,92±0,92 |
0,231 |
|
Créatininémie (mg/l) |
11±3 |
18,1±6 |
0,081 |
|
DFG (ml/min/1,73 m²) |
73±16 |
50±14 |
0,167 |
|
BNP (pg/ml) |
4436±8371 |
7582±11716 |
0,275 |
|
Natrémie (meq/l) |
137±3 |
139±1 |
0,87 |
|
CRP (mg/l) |
65±54 |
45±29 |
0,532 |
|
FEVG (%) |
26±8 |
23±6 |
0,395 |
|
DTSVG (mm) |
50±8 |
57±8 |
0,562 |
|
DTDVG (mm) |
60±9 |
65±8 |
0,645 |
|
FSVD Altérée (%) |
25 |
50 |
0,163 |
|
E/A |
2±1,33 |
2,1±1,18 |
0,814 |
|
E/Em |
21±21 |
14±2 |
0,656 |
|
PAPS (mmHg) |
48±22 |
33±10 |
0,012 |
|
Distance TDM6≤250 (%) |
25 |
64,3 |
0,037 |
|
Distance parcourue (m) |
335±75 |
235±108 |
0,047 |
|
PAS (mmHg) |
117±9 |
116±22 |
0,485 |
|
PAD (mmHg) |
73±11 |
80±18 |
0,693 |
|
Fc (bpm) |
104±15 |
88±28 |
0,475 |
BB : bétabloquant, BBG : bloc de branche gauchem ; BNP: B-type natriuretic peptide; CRP : protéine C-réactive; DFG : débit de filtration glomérulaire ; DTDVG : diamètre télédiastolique du ventricule gauche; DTSVG : diamètre télésystolique du ventricule gauche; ESV : extrasystole ventriculaire; FA : fibrillation auriculaire; Fc : fréquence cardiaque; FEVG : fraction éjection du ventricule gauche; FSVD : fonction systolique du ventricule droit; HTA : hypertension artérielle; IC : insuffisance cardiaque; IEC : inhibiteur de l'enzyme de conversion, ISGLT2: Sodium-glucose transport protein 2 inhibitors; NYHA: new york heart association; PAD : pression artérielle diastolique; PAPS: pression artérielle pulmonaire systolique, PAS : pression artérielle systolique; TDM6 : test de marche de six minutes
Tableau 7
Analyse univariée COX qui prédit la réhospitalisation chez les patients hospitalisés pour insuffisance cardiaque à FEVG réduite
|
Caractéristiques des patients |
Wald test |
HR |
95% CI |
P-value |
|
Age (ans) |
3,779 |
1,035 |
1-1,071 |
0,052 |
|
Les hommes |
1,541 |
30,158 |
0,139-6531 |
0,214 |
|
Antécédant IC (%) |
1,573 |
1,972 |
0,682-5,696 |
0,210 |
|
PAS |
0,665 |
0,988 |
0,960-1,017 |
0,415 |
|
PAD |
3,514 |
0,956 |
0,911-1,002 |
0,061 |
|
Fc (bpm) |
0,312 |
0,99 |
0,954-1,026 |
0,577 |
|
FA (%) |
1,552 |
0,499 |
0,167-1,490 |
0,213 |
|
ESV % |
0,032 |
1,123 |
0,313-4,029 |
0,858 |
|
Urémie (g/l) |
1,248 |
1,797 |
0,642-5,028 |
0,264 |
|
Créatininémie (mg/l) |
2,379 |
1,079 |
0,98-1,187 |
0,123 |
|
DFG (ml/min/1,73 m²) |
2,650 |
0,977 |
0,950-1,005 |
0,104 |
|
BNP (pg/ml) |
0,051 |
1 |
1-1 |
0,821 |
|
CRP (mg/l) |
0,72 |
1,002 |
0,989-1,014 |
0,788 |
|
FEVG (%) |
1,114 |
1,045 |
0,963-1,133 |
0,291 |
|
DTSVG (mm) |
1,182 |
0,963 |
0,899-1,031 |
0,277 |
|
DTDVG (mm) |
1,223 |
0,963 |
0,902-1,029 |
0,269 |
|
FSVD Altérée (%) |
2,736 |
0,412 |
0,144-1,178 |
0,098 |
|
E/A |
0,294 |
0,854 |
0,482-1,512 |
0,588 |
|
E/Em |
0,02 |
0,999 |
0,958-1,042 |
0,963 |
|
PAPS (mmHg) |
3,866 |
0,974 |
0,949-1 |
0,049 |
|
Distance parcourue (m) |
6,521 |
4,193 |
1,396-12,599 |
0,011 |
|
Distance TDM6 ≤250 |
6,321 |
0,993 |
0,987-0,988 |
0,012 |
|
PAS après TDM6 |
0,672 |
0,988 |
0,959-1,017 |
0,412 |
|
PAD après TDM6 |
0,015 |
0,998 |
0,962-1,035 |
0,902 |
|
Fc après TDM6 |
0,441 |
0,990 |
0,961-1,020 |
0,507 |
BB : bétabloquant, BBG : bloc de branche gauchem ; BNP: B-type natriuretic peptide; CRP : protéine C-réactive; DFG : débit de filtration glomérulaire ; DTDVG : diamètre télédiastolique du ventricule gauche; DTSVG : diamètre télésystolique du ventricule gauche; ESV : extrasystole ventriculaire; FA : fibrillation auriculaire; Fc : fréquence cardiaque; FEVG : fraction éjection du ventricule gauche; FSVD : fonction systolique du ventricule droit; HTA : hypertension artérielle; IC : insuffisance cardiaque; IEC : inhibiteur de l'enzyme de conversion, ISGLT2: Sodium-glucose transport protein 2 inhibitors; NYHA: new york heart association; PAD : pression artérielle diastolique; PAPS: pression artérielle pulmonaire systolique, PAS : pression artérielle systolique; TDM6 : test de marche de six minutes
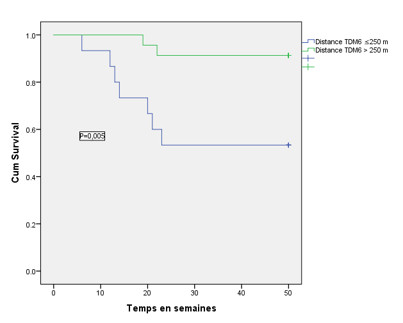
Figure 2: Probabilité de décès des patients en fonction de la distance du TDM6 (courbe de Kaplan-Meier).
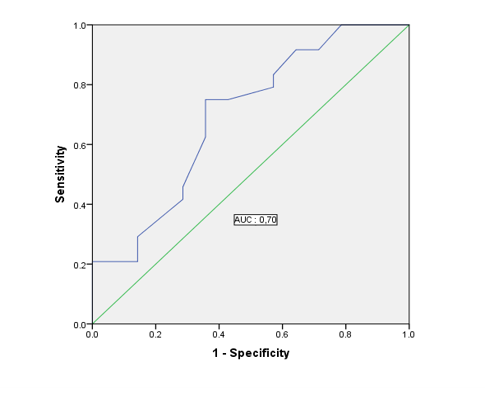
Figure 3: Courbe ROC. Area under the curve (AUC) = 0.7; 95% CI = 0.51 – 0.87; p =0,049. The optimal cut-point distance = 250 m with a sensitivity of 0.75 and specificity of 0.64
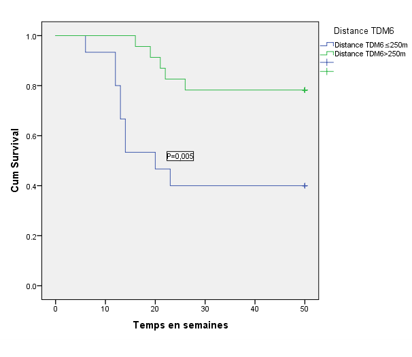
Figure 4: Probabilité de rehospitalisation pour insuffisance cardiaque des patients en fonction de la distance du TDM6 (courbe de Kaplan-Meier).
REFERENCES
1. Roger VL. Epidemiology of Heart Failure: A Contemporary Perspective. Circ Res. 14 mai 2021;128(10):1421‑34.
2. Bozkurt B, Coats AJS, Tsutsui H, Abdelhamid CM, Adamopoulos S, Albert N, et al. Universal definition and classification of heart failure: a report of the Heart Failure Society of America, Heart Failure Association of the European Society of Cardiology, Japanese Heart Failure Society and Writing Committee of the Universal Definition of Heart Failure: Endorsed by the Canadian Heart Failure Society, Heart Failure Association of India, Cardiac Society of Australia and New Zealand, and Chinese Heart Failure Association. Eur J Heart Fail. mars 2021;23(3):352‑80.
3. Heidenreich PA, Bozkurt B, Aguilar D, Allen LA, Byun JJ, Colvin MM, et al. 2022 AHA/ACC/HFSA Guideline for the Management of Heart Failure: A Report of the American College of Cardiology/American Heart Association Joint Committee on Clinical Practice Guidelines. Circulation [Internet]. 3 mai 2022 [cité 4 juin 2024];145(18). Disponible sur: https://www.ahajournals.org/doi/10.1161/CIR.0000000000001063
4. Stewart S, MacIntyre K, Hole DJ, Capewell S, McMurray JJV. More ‘malignant’ than cancer? Five‐year survival following a first admission for heart failure. Eur J Heart Fail. juin 2001;3(3):315‑22.
5. Mamas MA, Sperrin M, Watson MC, Coutts A, Wilde K, Burton C, et al. Do patients have worse outcomes in heart failure than in cancer? A primary care‐based cohort study with 10‐year follow‐up in Scotland. Eur J Heart Fail. sept 2017;19(9):1095‑104.
6. Cohn JN, Rector TS. Prognosis of congestive heart failure and predictors of mortality. Am J Cardiol. 1988;62(2):25A-30A.
7. Pilote L, Silberberg J, Lisbona R, Sniderman A. Prognosis in patients with low left ventricular ejection fraction after myocardial infarction. Importance of exercise capacity. Circulation. déc 1989;80(6):1636‑41.
8. Mancini D, LeJemtel T, Aaronson K. Peak V̇ O 2: A Simple yet Enduring Standard. Circulation. 14 mars 2000;101(10):1080‑2.
9. Bittner V, Weiner DH, Yusuf S, Rogers WJ, McIntyre KM, Bangdiwala SI, et al. Prediction of mortality and morbidity with a 6-minute walk test in patients with left ventricular dysfunction. SOLVD Investigators. JAMA. 13 oct 1993;270(14):1702‑7.
10. Rostagno C, Olivo G, Comeglio M, Boddi V, Banchelli M, Galanti G, et al. Prognostic value of 6‐minute walk corridor test in patients with mild to moderate heart failure: comparison with other methods of functional evaluation. Eur J Heart Fail. juin 2003;5(3):247‑52.
11. Curtis JP, Rathore SS, Wang Y, Krumholz HM. The association of 6-minute walk performance and outcomes in stable outpatients with heart failure. J Card Fail. févr 2004;10(1):9‑14.
12. Cahalin LP, Mathier MA, Semigran MJ, Dec GW, DiSalvo TG. The Six-Minute Walk Test Predicts Peak Oxygen Uptake and Survival in Patients With Advanced Heart Failure. Chest. août 1996;110(2):325‑32.
13. Faggiano P, D’Aloia A, Gualeni A, Brentana L, Cas LD. The 6 minute walking test in chronic heart failure: indications, interpretation and limitations from a review of the literature. Eur J Heart Fail. oct 2004;6(6):687‑91.
14. Fan Y, Gu X, Zhang H. Prognostic value of six-minute walk distance in patients with heart failure: A meta-analysis. Eur J Prev Cardiol. avr 2019;26(6):664‑7.
15. Roul G, Germain P, Bareiss P. Does the 6-minute walk test predict the prognosis in patients with NYHA class II or III chronic heart failure? Am Heart J. sept 1998;136(3):449‑57.
16. Forman DE, Arena R, Boxer R, Dolansky MA, Eng JJ, Fleg JL, et al. Prioritizing Functional Capacity as a Principal End Point for Therapies Oriented to Older Adults With Cardiovascular Disease: A Scientific Statement for Healthcare Professionals From the American Heart Association. Circulation [Internet]. 18 avr 2017 [cité 4 juin 2024];135(16). Disponible sur: https://www.ahajournals.org/doi/10.1161/CIR.0000000000000483
17. Alahdab MT, Mansour IN, Napan S, Stamos TD. Six Minute Walk Test Predicts Long-Term All-Cause Mortality and Heart Failure Rehospitalization in African-American Patients Hospitalized With Acute Decompensated Heart Failure. J Card Fail. mars 2009;15(2):130‑5.
18. Rubim VSM, Drumond Neto C, Romeo JLM, Montera MW. Valor prognóstico do teste de caminhada de seis minutos na insuficiência cardíaca. Arq Bras Cardiol [Internet]. févr 2006 [cité 4 juin 2024];86(2). Disponible sur: http://www.scielo.br/scielo.php?script=sci_arttext&pid=S0066-782X2006000200007&lng=pt&nrm=iso&tlng=pt
19. Shah MR, Hasselblad V, Gheorghiade M, Adams KF, Swedberg K, Califf RM, et al. Prognostic usefulness of the six-minute walk in patients with advanced congestive heart failure secondary to ischemic or nonischemic cardiomyopathy. Am J Cardiol. nov 2001;88(9):987‑93.
20. Naïbé Dangwé, T, Mandi Dakaboué, G, Bamouni. Six-Minute Walk Test Distance and Outcome in Patients with Chronic Heart Failure. Cardiologue à Tunis. 14e éd. 2018;91‑6.
21. Arslan S, Erol MK, Gundogdu F, Sevimli S, Aksakal E, Senocak H, et al. Prognostic value of 6-minute walk test in stable outpatients with heart failure. Tex Heart Inst J. 2007;34(2):166‑9.
22. Opasich C. Six-minute walking performance in patients with moderate-to-severe heart failure; is it a useful indicator in clinical practice? Eur Heart J. 15 mars 2001;22(6):488‑96.
23. Lucas C, Stevenson LW, Johnson W, Hartley H, Hamilton MA, Walden J, et al. The 6-min walk and peak oxygen consumption in advanced heart failure: Aerobic capacity and survival. Am Heart J. oct 1999;138(4):618‑24.
24. Guyatt GH, Sullivan MJ, Thompson PJ, Fallen EL, Pugsley SO, Taylor DW, et al. The 6-minute walk: a new measure of exercise capacity in patients with chronic heart failure. Can Med Assoc J. 15 avr 1985;132(8):919‑23.
25. Matsumoto K, Xiao Y, Homma S, Thompson JLP, Buchsbaum R, Ito K, et al. Prognostic impact of 6 min walk test distance in patients with systolic heart failure: insights from the WARCEF trial. ESC Heart Fail. avr 2021;8(2):819‑28.
26. McCabe N, Butler J, Dunbar SB, Higgins M, Reilly C. Six-minute walk distance predicts 30-day readmission after acute heart failure hospitalization. Heart Lung. juill 2017;46(4):287‑92.
27. Bader F, Atallah B, Brennan LF, Rimawi RH, Khalil ME. Heart failure in the elderly: ten peculiar management considerations. Heart Fail Rev. mars 2017;22(2):219‑28.
28. Ferreira JP, Metra M, Anker SD, Dickstein K, Lang CC, Ng L, et al. Clinical correlates and outcome associated with changes in 6‐minute walking distance in patients with heart failure: findings from the BIOSTAT‐CHF study. Eur J Heart Fail. févr 2019;21(2):218‑26.
29. Arhlade F, Sabri F, Nassiri I, Asadi A, Habbal R. 0432: Six minute walk test: predictor of hospital readmission in patients with chronic heart failure. Arch Cardiovasc Dis Suppl. janv 2016;8(1):27.
30. Andersson B, Waagstein F. Spectrum and outcome of congestive heart failure in a hospitalized population. Am Heart J. sept 1993;126(3):632‑40.

